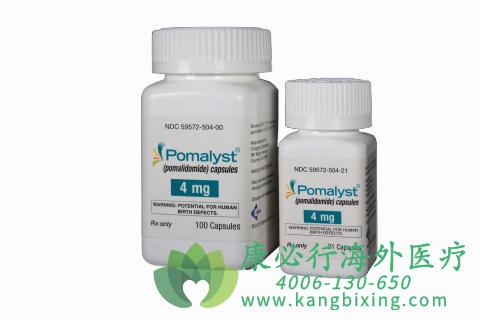
���������Ȱ�(POMALIDOMID)��������Ʒ����ΪPomalyst ����ŷ�˺Ͷ���˹Ʒ����Imnovid������Celgene���۵�ɳ���Ȱ�������������п�Ѫ���������ã�Ҳ����Ϊ���ߵ��ڼ���2013��2�£�Pomalidomide������ʳƷ��ҩ������֣�FDA�����������Ƹ����������Զ�Թ����������ѱ��������Ѿ���������������ǰ�Ʒ����ˣ��������ǶȰ����������ף����������һ��������ɺ�60���֮��֤ʵ�˼�����չ������2013��8�»����ŷ��ίԱ�����������
����ɳ���Ȱ��������������������Ӧ���ڽ��ܹ�����2�ּ������ƣ��������ǶȰ��͵���ø�����Ƽ����Ļ��ߵĶ�Թ����������������һ��������ɺ�60���֮���м�����չ���ظ���28�����ڵĵ�1-21�죬4mg �ڷ� ÿ��1��ֱ��������չ;��ͼ���������������ʹ��
�����ͼ�����������
��������ÿ��28�����ڵĵ�1,8,15��22�����ڷ�
������75�꣺40����/��
����> 75�꣺20����/��
������������
�����������������1 mg������������ԣ���ֹͣ����
����������ϸ������
����ANC <500 / mcL������������ϸ������֢�������ȡ�38.5��C��ANC <1,000 / mcL�������ANC�ָ�����500/ mcL,�ж����Ʋ�ÿ����ѭCBC,�ɻָ�3 mg /��
��������ÿ�������½�<500 / mcL:�ж����ƣ����ANC�ָ�����500/ mcL,���Իָ�����ǰ������1 mg
����ѪС�����
����ѪС��<25,000 / mcL:�ж����Ʋ�ÿ����ѭCBC,���ѪС��ָ�����50,000/ mcL,�ɻָ�3 mg /��
��������ÿ�������½�<25,000 / mcL:�ж����ƣ����ѪС��ָ�����50,000/ mcL,���Իָ�����ǰ������1 mg
��������
��������ֹͣѪ����ˮ�ף�Ƥ��ȥ���ʣ�������κ��������ص�Ƥ������Ӧ
������������3����4�����ԣ���ҽ��������������ѽ����С�ڻ����2��ʱ���������Ʋ����¿�ʼ���ƣ���֮ǰ�ļ�������1 mg
�������������
�������Ѫ�弡��> 3 mg / dL,�����ʹ��
�������Ѫ�嵨����> 2 mg / dL��AST / ALT> 3x ULN,�����ʹ��.�综����Ҫ������ѯ�����к���ҽ��ҽѧ���ʣ�4006-130-650��ɨ�������·���ά�룡

��������ҩƷ��������� �����Ȱ�(POMALIDOMID) https://www.kangbixing.com/drug/pmda/



 ���ӿ����й��ʣ����ʾ���
���ӿ����й��ʣ����ʾ���