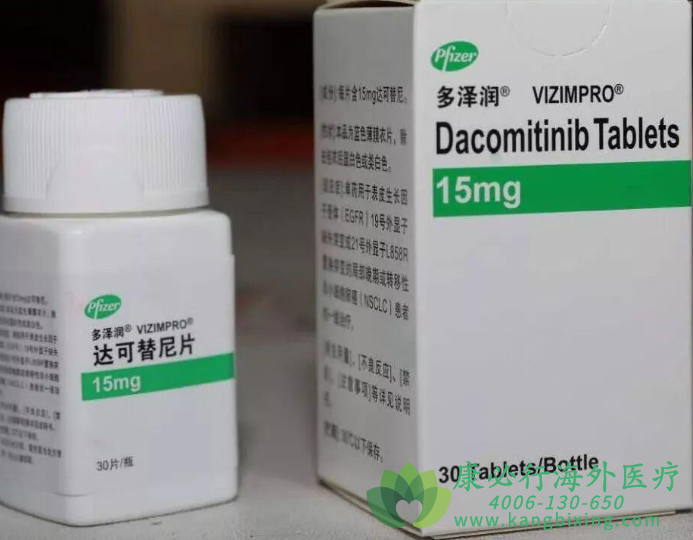
������ǰ��FDA������EGFR���Ƽ�Dacomitinib��Ϊһ���Ʒ����ڷ�Сϸ���ΰ���NSCLC�����ơ�Dacomitinib���ڶ���EGFR�Ұ��ἤø���Ƽ�����ҩ������������ʾ������EGFRͻ��NSCLC����ʱ�ȵ�һ��ҩ���簢˹��������ɳ����������������Ч������������ҩ�Է�����������ơ�Dacomitinib��λ�������Ʒ��Ϊvizimpro,��ҩ���ѻ�������������19ȱʧ��������21 L858R���EGFRͻ���NSCLC���ߡ�
����vizimpro�Ļ���������һЩ���ۣ���ҩ����2014�걨��������3��������δ�ﵽ�յ㡣�������������������ù�˾��չ�˵��������飨ARCHER 1050����ȥ��������������˻����Ľ����������ʾvizimpro������ɳ��ȣ�ʹ��չ�����ڣ�PFS����9.2�����ӳ���14.7���£������������չ���������ս�����41%��
����vizimpro���ڽ�����һ����������ս����ɳ�����������µİ������ᡣ������ҩ���������ս���ǰ�˹������Tagrisso��osimertinib�������߱�����Ϊһ����������Ƽ�������4�¸�ҩ���FDA������EGFR����NSCLCһ�����ơ�
����Tagrisso��ȷ�������������EGFR����NSCLC���ȹ̵�λ���ڻ���һ��ҩ��֮ǰ����ȥ������۶�ߴ�10����Ԫ����˹����ǿ������TagrissoӦ����ҩ֮ǰʹ�ã����ƺ��Ѿ���óɹ��������ϰ��꣬����Ϊһ��ҩ���Ӧ�ð��������۶�����89%���ﵽ7.6����Ԫ��
����vizimpro�ܷ���Tagrisso֮ǰʹ���Դ��ڼ������ѡ�ARCHER 1050����Ч�����ݹ�Ȼ�dz���ɫ����һЩ�ٴ�ҽ�����Ͽɰ�˹������Tagrisso,��Ϊ��ҩ����FLAURA�����е���ֵ��չ������Ϊ19���£�����һЩҽ����ΪTagrisso�������Ը��á��综����Ҫ������ѯ�����к���ҽ��ҽѧ���ʣ�4006-130-650��ɨ�������·���ά�룡

��������ҩƷ��������� vizimpro https://www.kangbixing.com/



 ���ӿ����й��ʣ����ʾ���
���ӿ����й��ʣ����ʾ���