HPV和癌症时代
1928年:
George Papanicolaou博士发现宫颈癌细胞可以通过阴道涂片检测来检测。这为他创造了世界上第一个宫颈癌筛查试验的方法,现在被称为“pap”涂片,它从宫颈而不是阴道擦拭细胞。
1943年:
该pap被介绍给医生办公室。它可以帮助医生检测和治疗子宫颈癌和癌前期,然后才能传播到其他器官。在接下来的几十年里,pap测试有助于防止高收入国家的数千人死亡。自首次引入以来,pap涂片导致了美国子宫颈癌发生率下降了约70%。

1983- 1985年:
德国研究人员发现大多数子宫颈癌前期和癌症都含有HPV。他们特别发现HPV 16型或18型。其他类型的HPV随后与子宫颈癌相关,但16和18被认为是最危险的。在20世纪80年代,HPV与肛门,阴茎,阴道和外阴癌的联系也被发现。
1990年:
首先将HPV16型和18型与口咽部癌症相关联的一些研究发表。
1999年:
65岁以上妇女进行的医疗补贴筛查对宫颈癌进行了广泛的筛查,导致了1990年以来该癌症诊断率的下降了19%。筛查使癌前病变发生更多的检测,导致早期治疗,阻止癌症的发展。
1999年:
HPV DNA检测由FDA批准。它与pap涂片不同,因为它使用特定的机器在细胞的DNA中寻找高危HPV DNA的存在,而pap涂片通过显微镜观察细胞的异常变化。HPV DNA测试能够鉴定几种高危HPV类型的DNA。HPV检测可以检测出有可能引起细胞异常的HPV感染,有时甚至在这些异常甚至可见之前。
HPV检测目前被批准用于25岁以上的女性,而不需要同时进行pap检查,也可以为任何年龄段的女性进行异常pap检查。单独使用,HPV检测将有助于确定是否需要额外的检测或筛选。HPV检测比pap检测更好地检测癌前病变,但也能产生更多的假阳性。综合来说,DNA和pap测试是检测癌前风险的优良工具。在2014年,FDA批准了单独使用HPV DNA检测来检测癌前病变,并确定需要进行额外的检测。
2006年:
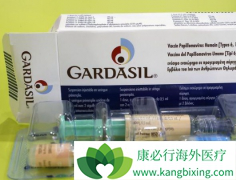
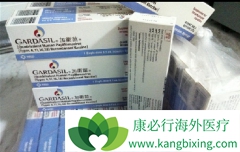
FDA批准Gardasil,这是第一个防止HPV感染的疫苗。Gardasil的这个第一版可以预防HPV16和18感染,这两种引起大多数肛门,阴道,外阴,口咽,阴茎和子宫颈癌的高风险菌株。它被批准用于9-26岁的女性和男性,但是,这个时候只是常规推荐给女孩。在2009年,男孩们被允许推荐。
2008年:
针对HPV16和18号称为Cervarix的第二种疫苗在英国被批准为9-25岁的女性。

2009年:
Cervarix被批准在美国10-25岁的女性。Gardasil也被批准在9-26岁的男性在美国使用,以防止生殖器疣。
2010:
FDA批准Gardasil预防肛门癌。HPV和肛门癌基金会在FDA之前就防止肛门癌的重要性作证。
2011:
在美国,凡尔赛尔通常推荐给11-12岁的所有儿童 - 男孩和女孩。这意味着推荐给所有的孩子在与青春期前疫苗Tdap和脑膜炎球菌一起检查之前进行。男婴的推荐疫苗最多为21岁,尚未接种疫苗的女孩为26岁。建议男性与男性和免疫功能低下的男性接种疫苗直到26岁。在CDC举行的听证会上,HPV和肛肠癌基金会领导组织联盟提交多份证词,以支持扩大疫苗可保护所有儿童免受HPV及其引起的癌症。在这里和这里阅读这些证词。
2012:
英国卫生部批准Gardasil,并取代了Cervarix在国家免疫方案。
2013:
总统癌症小组发布了一份报告,呼吁增加疫苗接种量。小组注意到,2012年,少女少女的疫苗覆盖率仅为33.4%。男孩中的覆盖率甚至更差,只有6.8%。小组认为这些低利率是“对癌症进展的严重威胁”小组说:“通过支持疫苗接种作为国家和全球卫生的紧急优先事项,美国国家癌症计划有前所未有的机会,有助于预防数百万可避免的癌症和全球男女的其他条件“。
2014:
ANCHOR研究开始了。本研究旨在确定艾滋病毒+男性和女性高级鳞状上皮内病变(HSIL)的常规筛查和治疗是否是预防肛门癌的有效方法。这项研究仍在积极招募参与者。HPV和肛门癌基金会希望有一天的肛门涂片会像今天的颈部鳞屑一样常规。ANCHOR的研究是朝着这一天迈出的第一步,每年挽救数千人的生命。请阅读我们给国家癌症研究所的信件,以支持这里 和 这里的这项研究。
同样在2014年,FDA批准使用第三种疫苗Gardasil 9,用于9-26岁的女性和9-15岁的男性。加入“9”,因为这种疫苗可以为9种不同的HPV类型提供保护:6,11,16,18,31,33,45,52和58.像Gardasil一样,Gardasil 9可防止肛门,宫颈,外阴和阴道癌; 6型和11型防止生殖器疣。请参阅我们的疫苗接种页面了解更多信息,了解有关防治HPV的最新补充信息。预计这项建议将会扩大到包括2015年底或2016年底的所有女孩和男孩达26人。



 添加康必行顾问,想问就问
添加康必行顾问,想问就问