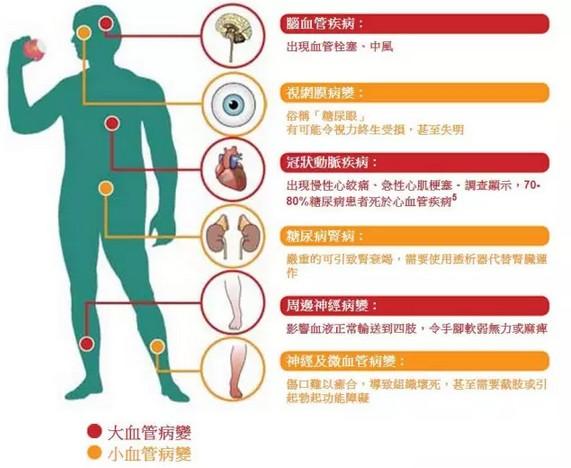
替尔泊肽(Tirzepatide)是首个且目前唯一的葡萄糖依赖性促胰岛素多肽(Glucose-dependent InsulinotropicPeptide,GIP)和胰高血糖素样肽-1(Glucagon-Like Peptide-1,GLP-1)受体激动剂,商品名Mounjaro。GLP-1和GIP都属于肠促胰素,由人体胃肠道黏膜分泌的多肽,前者可与胰岛细胞上的受体结合并刺激胰岛素分泌,进而产生降糖作用,还可延缓胃排空和抑制食欲,从而控制体重;而后者具有抑制胃酸、胃蛋白酶分泌、刺激胰岛素释放、抑制胃的蠕动和排空等功能,协同GLP-1受体激动剂作用。
一项多中心、随机、双盲、平行、安慰剂对照的III期临床研究,研究纳入肥胖(BMI≥28 kg/m2)或伴有至少一种合并症的超重(BMI≥24 kg/m2)的中国成人患者,旨在低热量饮食和增加运动的基础上对比替尔泊肽与安慰剂在体重减轻方面的有效性和安全性。研究入组了210名中国患者(基线体重均值为91.8kg、BMI均值为32.3 kg/m2),以1:1:1的比例随机分组,分别接受替尔泊肽10mg或15 mg或安慰剂每周一次治疗。
共同主要终点结果显示,治疗52周时,替尔泊肽10 mg和15 mg治疗组体重自基线的平均变化百分比分别为-14.4%和-19.9%,优效于安慰剂组(-2.4%);替尔泊肽组(10 mg,91.4%;15 mg,92.7%)达到体重减轻≥5%的患者比例优效于安慰剂组(29.4%)。此外,替尔泊肽组(10 mg,48.6%;15 mg,72.1%)达到体重减轻≥15%的患者比例也优效于安慰剂组(2.9%)。SURMOUNT-CN的结果将于2023年10月在欧洲糖尿病研究协会(EASD)学术年会上公布。
基于临床良好的结果,替尔泊肽注射液减重适应症的申报情况如下:
减重适应症已在美国FDA的注册申请获得快速通道资格,预计最早将于2023年底获批;
2022年9月在国内提交用于治疗II型糖尿病适应症的注册申请,预计24年上半年获批;
2023年8月21日,减重适应症的注册申请获中国药监局NMPA受理。如有需要,请咨询康必行海外医疗医学顾问:4006-130-650或扫码添加下方微信,我们将竭诚为您服务!
更多药品详情请访问 替尔泊肽 https://www.kangbixing.com/



 添加康必行顾问,想问就问
添加康必行顾问,想问就问