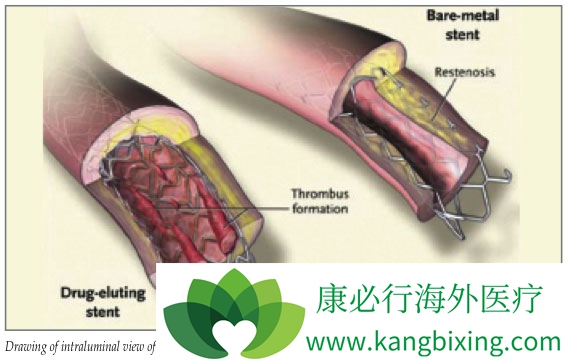
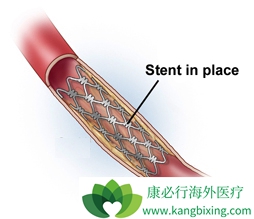
冠状动脉支架的出现一直是经皮冠状动脉介入治疗冠状动脉疾病的里程碑式发展。使用球囊血管成形术的初始经皮治疗由于立即血管弹性反冲和解剖以及晚期负血管重塑和新生内膜增生而引起的临床疗效有限。随着冠状动脉支架的引入,初始裸金属支架(BMS),消除了除了血管弹性反冲之外由于损伤引起的解剖和负重塑的问题;然而,新生内膜增生仍然是支架长期功效的持续障碍。新生内膜增生导致支架内再狭窄20%-30%的病例在BMS干预后,导致靶向病变血运重建率高。后来,引入药物洗脱支架(DES),其具有从支架释放抗增殖药物以减少新生内膜增殖的附加优点,从而导致支架内再狭窄率降低。虽然第一代DES与其前身相比有显着改善的结果,BMS仍然存在支架血栓形成和支架延迟内皮化等诸多挑战。第二代DES在功效和安全性方面比第一代前辈得到了显着改善,即改善了长期疗效,支架血栓形成明显减少。DES后双重抗血小板治疗的持续时间也在多次大型试验中得到广泛研究。新一代支架,包括具有生物可再吸收聚合物,无聚合物,而完全生物可吸收的支架仍处于发展的早期阶段。最后,关于使用冠状动脉支架与冠状动脉搭桥手术治疗复合/多血管冠状动脉疾病的多个试验中的持续加热比较继续发展。

经皮冠状动脉介入治疗的开始 - 常规球囊血管成形术
经皮冠状动脉介入(PCI)得到了大幅进化由于第一球囊冠状动脉腔内成形术是由安德烈亚斯·格鲁茨格于1979年进行1引入球囊冠状动脉腔内成形术,也被称为经皮腔内冠状动脉成形术,其随后也被称为“普通老式气囊血管成形术的(POBA)提供了使用非手术经皮形式的血运重建的历史性突破性医学概念作为冠状动脉旁路移植术(CABG)的替代策略1手术。然而,包括急性血管反冲和血管解剖在内的直接并发症,除了由于局灶性血管损伤引起的负面重塑和内膜增生等长期影响外,还会影响其疗效和安全性。大约40%的患者在6个月时发生血管造影显着的再狭窄,其中50%-75%具有复发性缺血症状。2因此,大约20%-30%的患者适当要求在球囊血管成形术后的第一年内重新进行指数病变血运重建。1年后复发性缺血症状主要是由于新的或进行性的病变。

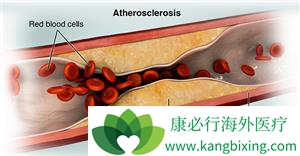
球囊血管成形术后再狭窄的病理生理学是由于以下因素的组合,包括:a)急性动脉反冲,b)冠状动脉夹层,c)阴性重塑,d)新生内膜增生。由于动脉壁在愈合过程中的收缩,负伤重建在受伤部分逐渐发生,并且与内皮与血流的相互作用也有关。新内膜增生发生在数周到数月之内,并且是平滑肌细胞(SMC)从中膜介质到内膜的增殖和迁移,导致侵入血管腔。5-8随后的出现和使用裸金属支架(BMS),前三个过程和/或其后遗症完全受到控制。然而,新生内膜增生的第四个因素仍然是BMS时代的一个重大挑战。9尽管新生内膜增生是球囊血管成形术后再狭窄的主要机制,但其是支架内再狭窄(ISR)的唯一机制,不包括支架扩张不足。因此,新生内膜增生的病理生理学非常重要,将在BMS部分进行全面讨论。



 添加康必行顾问,想问就问
添加康必行顾问,想问就问