适应症、临床疗效数据;每天两次在皮损区域涂抹薄层,最多为体表面积的10%(每周最多60克)。严重的副作用:包括严重的感染;非黑色素瘤皮肤癌;血栓形成;和血小板减少症、贫血症和中性粒细胞减少症。Opzelura产品标签带有黑框警告,表示严重感染会导致住院或死亡;更高的全因死亡率,包括心血管猝死;淋巴瘤和其他恶性肿瘤;较高的主要心血管不良事件发生率(包括心血管死亡、心肌梗塞和中风);血栓形成(包括深静脉血栓形成、肺栓塞和动脉血栓形成)。
常见的副作用:包括鼻咽炎、头痛、发热、耳部感染、应用部位痤疮、荨麻疹、毛囊炎、扁桃体炎和流涕。
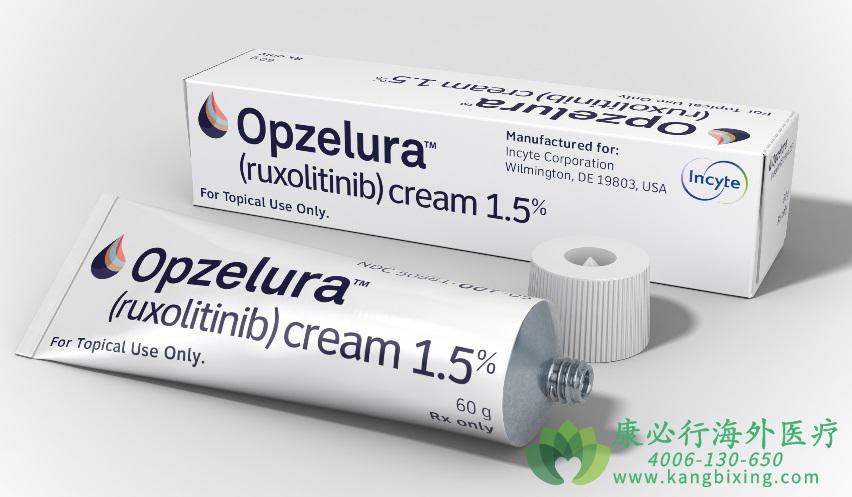
芦可替尼乳膏Opzelura(ruxolitinib)由Incyte公司研制,专为局部应用而设计。芦可替尼(鲁索替尼)的口服制剂于2011年首次以Jakafi品牌获批,用于治疗骨髓纤维化、真性红细胞增多症和移植物抗宿主病。
2021年9月21日,美国FDA批准Opzelura(ruxolitinib乳膏剂),用于短期和非持续性慢性治疗接受外用处方疗法未能充分控制病情或当这些疗法不可取、非免疫功能低下的轻度至中度特应性皮炎(AD)青少年(年龄≥12岁)和成人患者。
FDA基于两个三期临床试验数据(TRuE-V1 and TRuE-V2),于昨日批准了OPZELURA芦可替尼乳膏用于局部治疗成人和12岁及以上儿童患者的非节段性白癜风。两组试验共入组了12岁及以上共600多名非节段性白癜风患者,与安慰剂组对照评价OPZELURA的安全性和疗效。治疗24周时结果显示,OPZELURA治疗组比对照组明显改善了患者的VASI评分,患者面部和体表皮肤复色率都明显改善,并且这种改善在52周时一直持续且更为明显,52周再评估时:
75%的患者达到了F-VASI50,即皮损较基线改善大于等于50%;50%左右的患者达到了F-VASI75,即皮损较基线改善大于等于75%;
2022年7月18日(美国当地时间),FDA批准了Opzelura(ruxolitinib cream)1.5%芦可替尼(鲁索替尼)乳膏新适应症:用于局部治疗成人和12岁及以上儿童患者的非节段性白癜风。Opzelura是FDA批准的第一个也是唯一一个治疗白癜风的药物,也是唯一在美国批准的Janus激酶(JAK)抑制剂药物。白癜风是一种以皮肤色素脱失为特征的慢性自身免疫性疾病。芦可替尼乳膏获批为白癜风患者带来了新希望!
FDA批准Opzelura芦可替尼乳膏用于治疗白癜风;如有需要,请咨询康必行海外医疗医学顾问:4006-130-650或扫码添加下方微信,我们将竭诚为您服务!



 添加康必行顾问,想问就问
添加康必行顾问,想问就问