2019年04月09日,安进/UCB宣布FDA批准sclerostin单抗Evenity (romosozumab)上市,适应症为绝经后女性伴高骨折风险的骨质疏松症,Evenity成为全球首款获批上市的anti-sclerostin单克隆抗体药物,药物既能够加速骨形成又可以减少骨吸收。
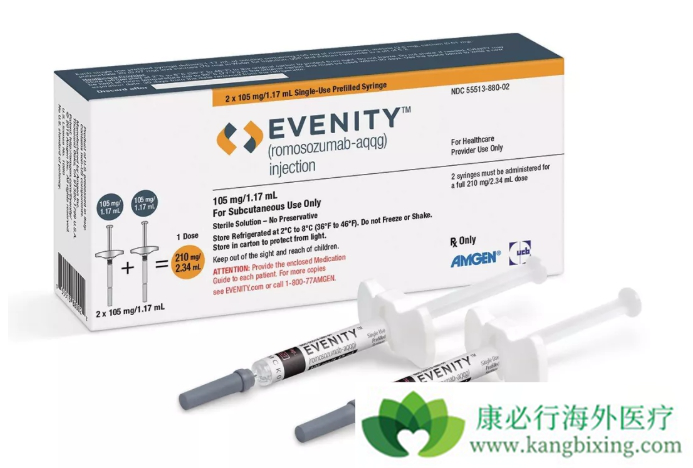
2019年01月08日,安进/UCB宣布日本厚生劳动省率先批准sclerostin单抗Evenity (romosozumab)上市,这是该款药物的一个重要里程碑事件。2019年04月09日,Evenity (romosozumab)终在美国获批,该药物的审评之路已经走过2年9个月。
事实上,2016年07月21日,安进/UCB已向FDA递交Evenity (romosozumab)上市申请,此次申请主要基于FRAME(NCT01575834)临床试验数据;2017年07月16日,FDA发出完全回复函,要求安进/UCB补充递交最新临床试验数据,即ARCH(NCT01631214);2018年07月12日,安进/UCB第2次向FDA递交Evenity (romosozumab)上市申请。



 添加康必行顾问,想问就问
添加康必行顾问,想问就问