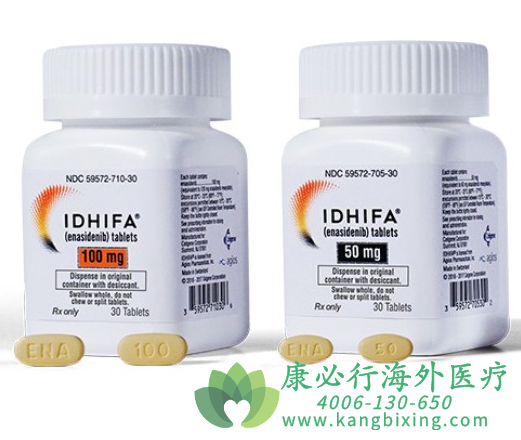
恩西地平的疗效,这些患者的IDH2突变是通过RealTime IDH2测定法检测出来的。该试验测量了没有疾病证据和治疗后血细胞完全恢复的患者(完全缓解或CR),以及没有疾病证据和治疗后血细胞部分恢复的患者(完全缓解与部分血液学恢复或CRh)的百分比。在至少6个月的治疗中,19%的患者经历了CR,中位数为8.2个月,4%的患者经历了CRh,中位数为9.6个月。在研究开始时因急性髓细胞白血病而需要输血或血小板的157名患者中,34%的人在使用恩西地平治疗后不再需要输血。
在一项公开标签、单臂、多中心的临床试验中,研究人员招募了199名成人患者,他们都患有复发性或难治性AML,且都带有IDH2突变。其中,至少有一半的患者曾接受过2项或更多的抗癌疗法。在研究中,患者们接受了每日100mg的初始剂量,直至病情出现进展,或出现无法接受的毒性。
研究表明,Idhifa能给患者带来完全缓解(CR),或是部分血液改善的完全缓解(CRh)。两者综合起来的数据是23%(n=46)(95%CI:18%,30%),中位数的缓解持续时间为8.2个月(95%CI:4.3,19.4)。
2017年8月1日,FDA批准了IDH2抑制恩西地平Enasidenib(IDHIFA)用于复发难治性成人急性髓系白血病的治疗。这是历史上第一个批准的与肿瘤代谢相关的一类抗癌新药。关于IDH2突变与肿瘤的相关性研究,首次报道于2006年Science杂志上,Sjöblom,Tobias等报道IDH突变与癌症的相关性,他们分析11例乳腺癌和11例结肠癌患者的13,023个基因,在一例结直肠癌患者中检出IDH突变。关于对此次获批的Idhifa疗效的研究中,对199例复发或难治性AML患者进行了单臂试验,这些患者在实时IDH2试验中发现了IDH2突变。该试验测量了没有疾病证据的患者的百分比和在治疗后完全恢复的血液计数(完全缓解或CR),以及没有疾病证据和部分恢复血液计数的患者(完全缓解部分的血液恢复或CRh)。
研究表明,携带IDH2突变的患者接受enasidenib至少有6个月的治疗时间后,19%的患者在CR中值为8.2个月,有4%的患者CRh的中值为9.6个月。在研究开始的时候,157名患者需要输血或血小板,而在Idhifa治疗后,34%的人不再需要输血。基于此项结果,FDA近日批准药物和伴随诊断上市。
对于这些患者来说,出现首次缓解的中位数时间为1.9个月(范围0.5个月到7.5个月不等),出现最佳缓解的中位数时间为3.7个月(范围0.6个月到11.2个月不等)。
Idhifa(Enasidenib)是异柠檬酸脱氢酶2(IDH2)的小分子抑制剂。Idhifa(Enasidenib)靶向突变体IDH2变体R140Q,R172S和R172K,其体外浓度比野生型酶低约40倍。在IDH2突变的AML小鼠异种移植模型中,Idhifa(Enasidenib)抑制IDH2酶,导致2-羟基戊二酸(2-HG)水平降低并诱导骨髓分化。在具有突变的IDH2的AML患者的血液样品中,Idhifa(Enasidenib)降低2-HG水平,减少细胞计数和增加成熟骨髓细胞的百分比。如有需要,请咨询康必行海外医疗医学顾问:4006-130-650或扫码添加下方微信,我们将竭诚为您服务!点击拓展阅读:恩西地平(ENASIDENIB/IDHIFA)的作用功效和使用方法
更多药品详情请访问 恩西地平 https://www.kangbixing.com/bxyw/exdp/



 添加康必行顾问,想问就问
添加康必行顾问,想问就问